A dos años y medio de la aparición del coronavirus que generó la actual pandemia por COVID-19 y a un año y medio del comienzo de la vacunación contra este patógeno, el mundo ya dispone de las primeras vacunas para la población pediátrica.
Esta mañana, la Agencia de Medicamentos de Estados Unidos (FDA, por sus siglas en inglés) autorizó el uso de urgencia de las vacunas de Pfizer y Moderna contra el COVID-19 en bebés y niños a partir de los 6 meses, allanando el camino para que desde la semana próxima se pueda comenzar a aplicar las primeras inyecciones.
La vacuna de Moderna, en dos dosis, está autorizada con carácter de urgencia para niños de entre seis meses y cinco años. La de Pfizer, esta vez en tres dosis, lo será entre los seis meses y los 4 años. Este es el último grupo de edad que aún no había recibido protección en Estados Unidos.
“Muchos padres, cuidadores y médicos han estado esperando una vacuna para niños más pequeños y esta acción ayudará a proteger a los menores de 6 meses de edad. Como hemos visto con los grupos de mayor edad, esperamos que las vacunas para los niños más pequeños brinden protección contra los resultados más graves del COVID-19, como la hospitalización y la muerte”, explicó el doctor Robert M. Califf, comisionado de la FDA.
 Las vacunas contienen componentes no activos de los virus, por lo que son completamente seguras, explicaron los expertos (Istock)
Las vacunas contienen componentes no activos de los virus, por lo que son completamente seguras, explicaron los expertos (Istock)
“Los padres pueden confiar en la seguridad y eficacia de estas vacunas contra el COVID-19 y pueden estar seguros de que la agencia fue minuciosa en su evaluación de los datos”, agregó el experto.
“Al igual que con todas las vacunas para cualquier población, al autorizarlas contra COVID-19 estas últimas destinadas a grupos de edad pediátrica, la FDA garantiza que nuestra evaluación y análisis de los datos sea riguroso y exhaustivo”, aclaró el doctor Peter Marks, director del Centro de Evaluación e Investigación Biológica de la FDA.
“Además de garantizar que los datos de estas vacunas cumplieran con los rigurosos estándares de la FDA, la convocatoria de un comité asesor por parte de la agencia fue parte de un proceso transparente para ayudar al público a tener una comprensión clara de los datos de seguridad y eficacia que respaldan la autorización de estas dos vacunas para poblaciones pediátricas”, concluyó el especialista.
Para la vacuna Moderna COVID-19, la FDA modificó la autorización de uso de emergencia (EUA, por sus siglas en inglés) para incluir el uso de la vacuna en personas de 6 meses a 17 años de edad. La vacuna había sido autorizada para su uso en adultos mayores de 18 años.
Para la vacuna Pfizer-BioNTech COVID-19, la FDA modificó la EUA para incluir el uso de la vacuna en personas de 6 meses a 4 años de edad. La vacuna había sido autorizada para su uso en personas de 5 años de edad y mayores.
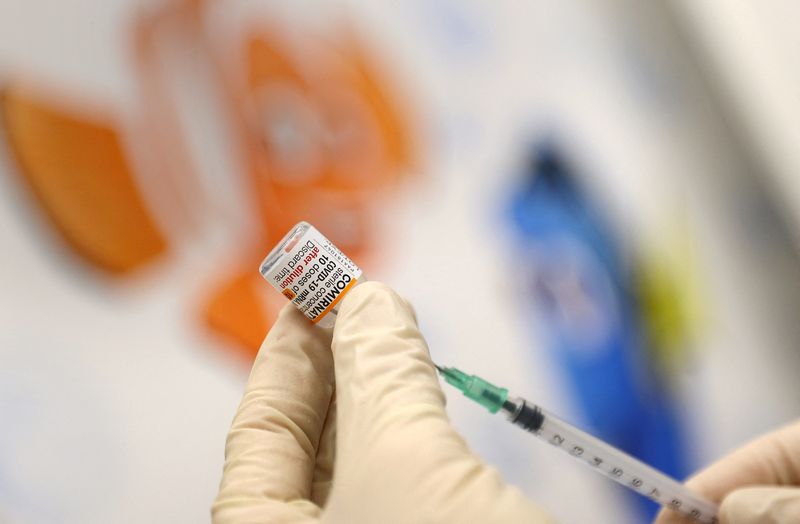 Los niños menores de 5 años conforman el último grupo que queda por recibir vacunas en Estados Unidos (REUTERS/Kai Pfaffenbach)
Los niños menores de 5 años conforman el último grupo que queda por recibir vacunas en Estados Unidos (REUTERS/Kai Pfaffenbach)
En diálogo exclusivo con Infobae, Rodrigo Sini de Almeida, desde San Pablo, Brasil, director de asuntos médicos de vacunas para América Latina de Pfizer, explicó detalles de uno de los varios ensayos clínicos en Fase I/II/III para la vacunación anti COVID en la población pediátrica, trabajo que el experto lideró.
El médico pediatra especializado en enfermedades infecciosas pediátricas y miembro de la Sociedad Brasileña de Pediatría y de la Sociedad Europea de Enfermedades Infecciosas Pediátricas, afirmó que los beneficios para la salud de la vacunación universal en niños y jóvenes menores de 18 años contra el COVID-19 no superan los riesgos potenciales.
10 razones para aprobar las vacunas COVID a partir de los 6 meses
1- La evaluación y el análisis de la FDA sobre la seguridad, la eficacia y los datos de fabricación de estas vacunas fueron rigurosos y completos, lo que respaldó estas autorizaciones de uso de emergencia.
2- La FDA determinó que los beneficios conocidos y potenciales de las vacunas Moderna y Pfizer-BioNTech contra el COVID-19 superan los riesgos conocidos y potenciales en las poblaciones pediátricas autorizadas para el uso de cada vacuna.
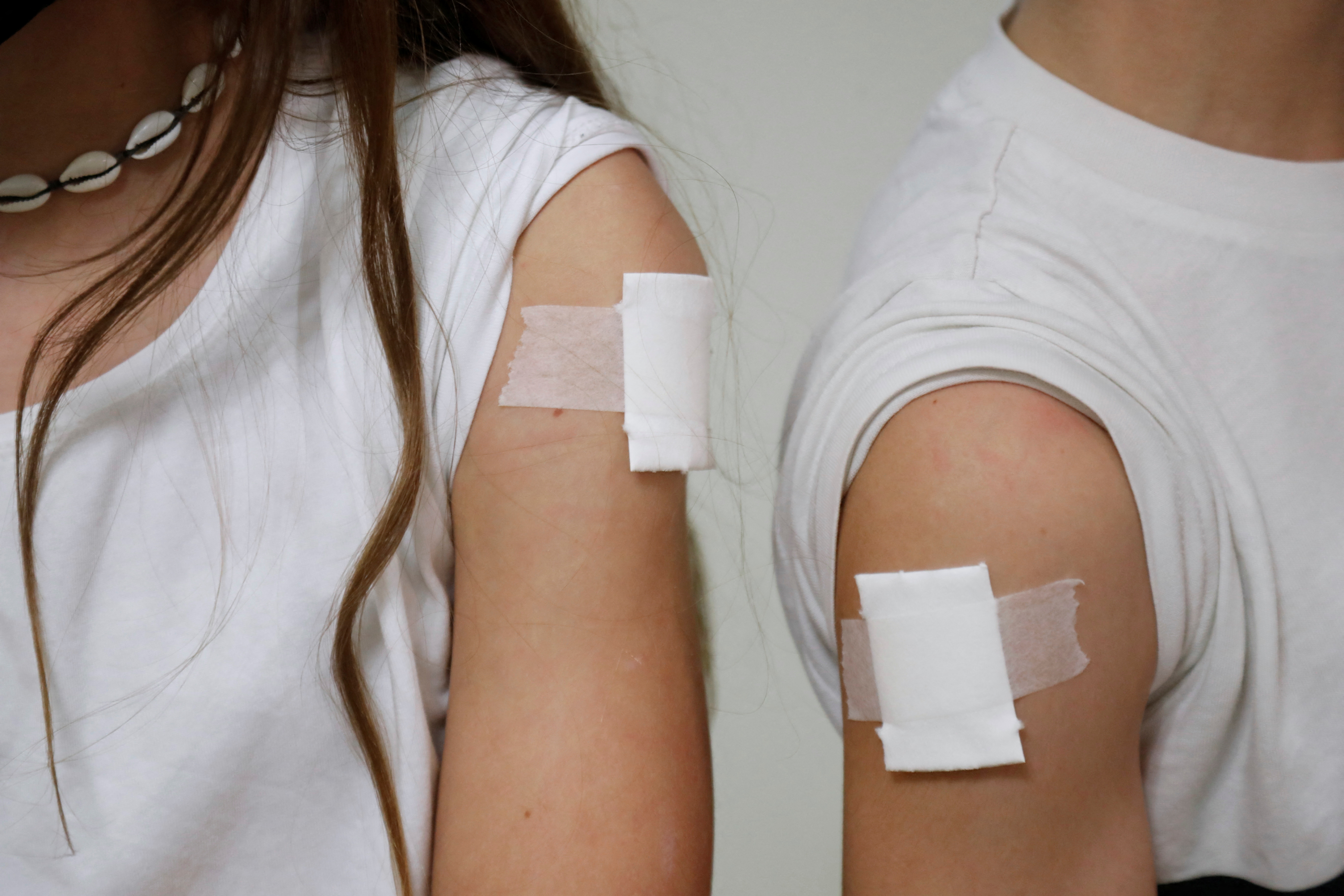 Los datos de efectividad y seguridad evaluados y analizados por la FDA llevaron meses de estudio (REUTERS/Susana Vera)
Los datos de efectividad y seguridad evaluados y analizados por la FDA llevaron meses de estudio (REUTERS/Susana Vera)
3- Antes de tomar la decisión de autorizar estas vacunas para las respectivas poblaciones pediátricas, se consultó al Comité Asesor de Vacunas y Productos Biológicos Relacionados de la FDA, que votó a favor de las autorizaciones.
4- Aunque únicamente cerca del 3% de los casos de COVID-19 en EEUU ocurren en niños de entre 6 meses y 4 años, las tasas de hospitalizaciones y decesos en ese grupo son mayores que en niños de más edad.
5- Los datos de efectividad y seguridad evaluados y analizados por la FDA para la vacuna Moderna COVID-19 para respaldar la EUA para estas poblaciones pediátricas se generaron en dos ensayos clínicos en curso, aleatorizados, ciegos, controlados con placebo en los Estados Unidos y Canadá que incluyeron bebés , niños y adolescentes.
6- La investigación realizada por Pfizer incluye a más de 5.400 participantes/voluntarios de diferentes partes del mundo que fueron divididos en tres grupos de edad: niños de 5 a 11 años, de 2 a 5 años y bebés de 6 meses a 2 años. Todos participantes niños de Estados Unidos, Finlandia, España y Polonia de 90 centros de salud.
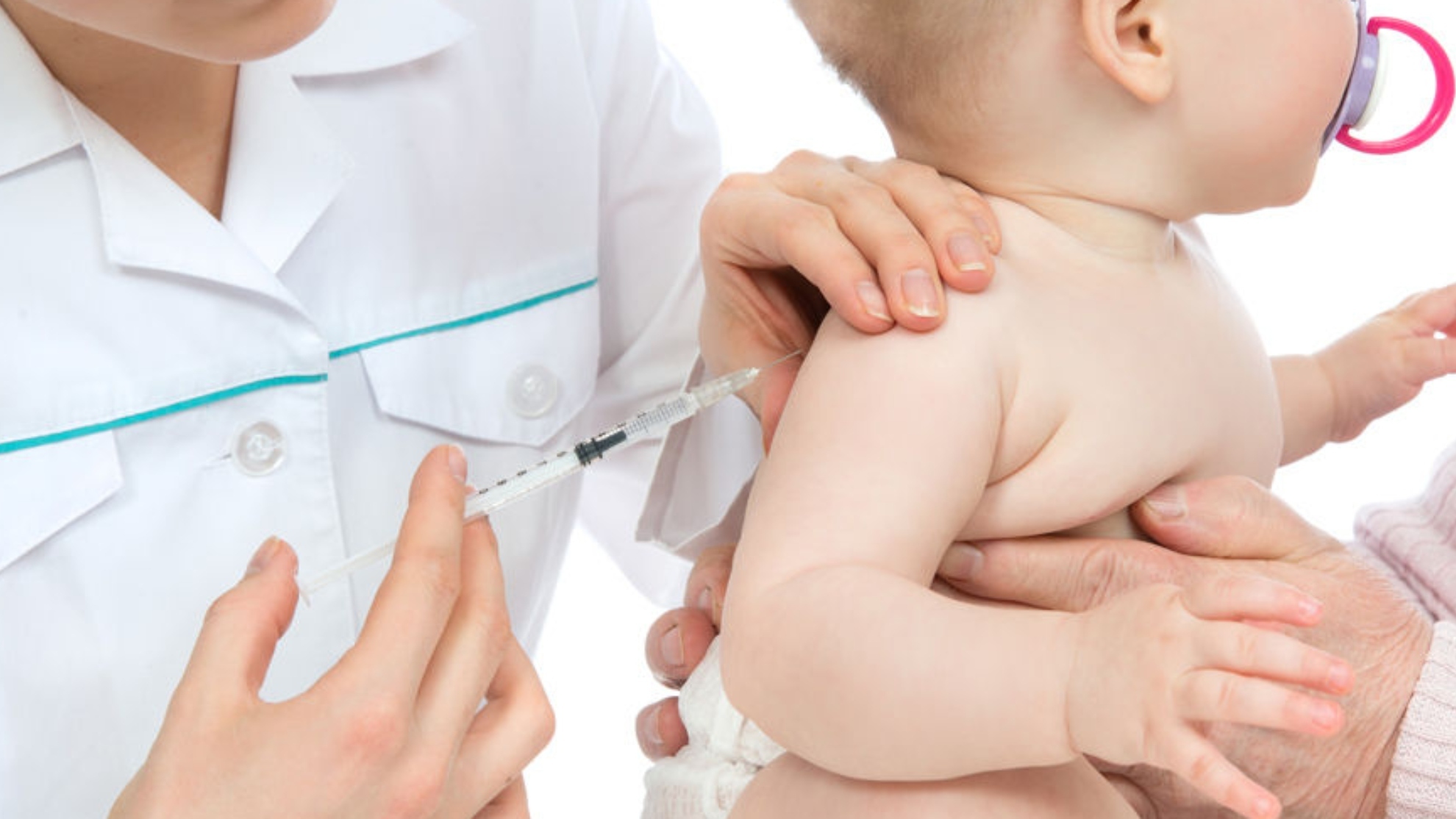 Muchos padres, cuidadores y médicos han estado esperando una vacuna para niños más pequeños y esta acción ayudará a proteger a los menores de 6 meses de edad (NHI)
Muchos padres, cuidadores y médicos han estado esperando una vacuna para niños más pequeños y esta acción ayudará a proteger a los menores de 6 meses de edad (NHI)
7- La FDA, que analizó de forma independiente los datos de los ensayos clínicos realizados por Moderna, dio cuenta de una eficacia contra los casos sintomáticos del 51% en bebés de 6 meses a 2 años, y del 37% en niños de 2 a 5 años. Aunque la eficacia de la vacuna en niños de 6 meses a 5 años de edad es menor que la observada en estudios en adultos y niños mayores, es consistente con la eficacia observada contra la variante Ómicron en adultos.
Sin embargo, la vacuna de Moderna en adultos, incluso con una efectividad reducida contra Ómicron, sigue siendo muy eficaz para proteger contra los casos graves de la enfermedad.
8- Respecto a Pfizer, “los datos disponibles apoyan la eficacia de la serie primaria de tres dosis de la vacuna contra el COVID-19 de Pfizer-BioNTech para prevenir el COVID-19 en el grupo de edad de 6 meses a 4 años. La vacuna Pfizer-BioNTech cumplió con el principal requisito de eficacia, ya que generó una respuesta inmunitaria al menos tan fuerte como la protección que la vacuna brinda a los adultos jóvenes.
La vacuna de Pfizer, aplicada en una serie de tres dosis, obtuvo una eficacia del 80,4% para evitar COVID-19 sintomático. La protección fue del 75,6% para bebés y niños pequeños de 6 a 23 meses, y del 82,4% para niños de 2 a 4 años. La cifra podría ajustarse en el futuro con los nuevos resultados del ensayo de Pfizer que está en curso.
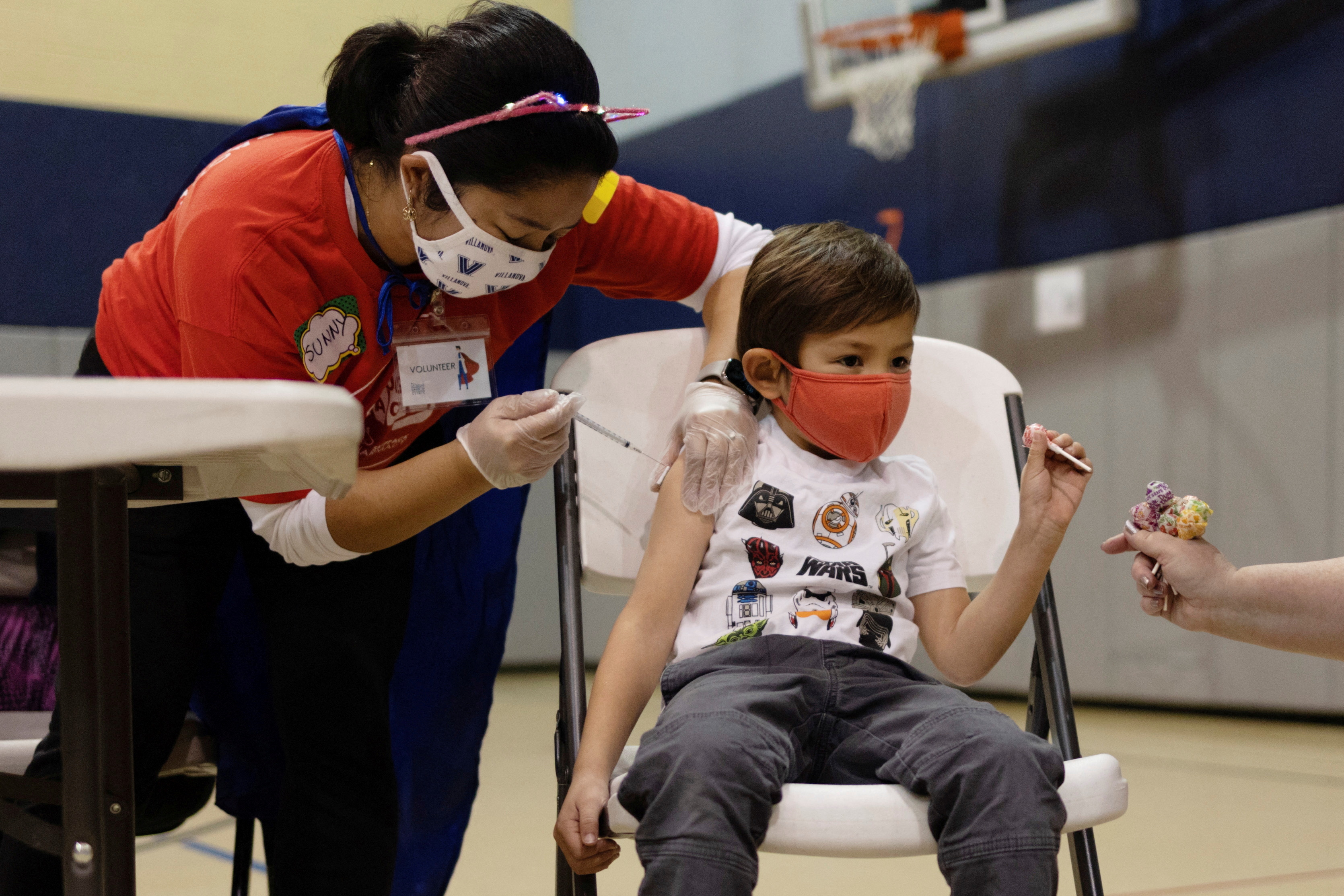 La FDA determinó que los beneficios conocidos y potenciales de las vacunas Moderna y Pfizer-BioNTech COVID-19 superan los riesgos conocidos y potenciales en las poblaciones pediátricas autorizadas para el uso de cada vacuna ( REUTERS/Hannah Beier/File Photo)
La FDA determinó que los beneficios conocidos y potenciales de las vacunas Moderna y Pfizer-BioNTech COVID-19 superan los riesgos conocidos y potenciales en las poblaciones pediátricas autorizadas para el uso de cada vacuna ( REUTERS/Hannah Beier/File Photo)
9- Los efectos secundarios para la vacuna de Moderna informados con mayor frecuencia en los participantes del ensayo clínico tanto para el grupo de edad de 6 a 11 años como para el grupo de edad de 12 a 17 años que recibieron la vacuna, incluyen dolor, enrojecimiento e hinchazón en el lugar de la inyección, cansancio, dolor de cabeza, dolor muscular, escalofríos , dolor en las articulaciones, ganglios linfáticos inflamados en la axila en el mismo brazo que la inyección, náuseas y vómitos y fiebre.
10- Los efectos secundarios informados con mayor frecuencia en los participantes de ensayos clínicos de Pfizer de 6 a 23 meses de edad que recibieron la vacuna fueron irritabilidad, disminución del apetito, fiebre y dolor, sensibilidad, enrojecimiento e hinchazón en el lugar de la inyección. Estos efectos secundarios también se informaron para los receptores de la vacuna de 2 a 4 años de edad.
Los niños menores de 5 años conforman el último grupo que queda por recibir vacunas en Estados Unidos. Unos 20 millones de chicos son hoy elegibles para recibir la inoculación. Habrá que ver si las vacunas se usan. Una encuesta reciente indicó que apenas uno de cada cinco padres iría inmediatamente a vacunar a sus hijos.
“Mientras más baja la edad, más baja es la tasa de vacunación”, declaró la doctora Lucía Abascal, del Departamento de Salud Pública de California. “Los chicos podrán empezar a ser inoculados el 21 de junio, dijo la semana pasada Ashish Jha, el coordinador de la Casa Blanca para la respuesta hacia la pandemia”.





